题目
有一包铜和碳组成的固体混合物,在一定条件下与氧气完全反应,生成固体氧化铜和二氧化碳气体,测得反应前后固体质量不变,则原固体混合物中碳的质量分数是
A.15%
B.20%
C.32%
D.无法确定
答案
B
解析
分析:铜与氧气反应生成氧化铜而使固体质量增大,碳与氧气反应生成气体二氧化碳而使固体质量减少;反应前后固体质量不变,则与铜反应的氧气的质量与混合物中碳质量相等,利用该等量关系,通过数据的假设进行计算.
解答:
假设混合物中碳的质量为m,则与铜反应氧气的质量为m,设混合物中铜的质量为x
2Cu+O2═2CuO
128 32
x m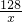 =
=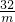 x=
x=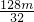
则原固体混合物中碳的质量分数=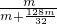 ×100%=20%
×100%=20%
故选B.
点评:分析得出与铜反应的氧气质量与混合固体中碳质量相等,是解决问题的前提,需要具备较强的分析能力.
